Химия ОГЭ 2020, часть 1. Задание 6 с комментариями экспертов (разбор задания № 6 на 3 примерах). Материал для подготовки к экзамену.
Вернуться к Списку экзаменационных заданий по химии
ОГЭ по химии. Разбор задания № 6
Ответами к заданиям 1–19 являются цифра или последовательность цифр.
Пример 1.
Какие два утверждения верны для характеристики как фосфора, так и алюминия?
- 1) Электроны в атоме расположены в трёх электронных слоях.
- 2) Соответствующее простое вещество существует в виде двухатомных молекул.
- 3) Химический элемент относится к металлам.
- 4) Значение электроотрицательности меньше, чем у серы.
- 5) Химический элемент образует высший оксид с общей формулой ЭO2.
Ответ: [ ].
Решение задания (с комментариями)
Базовые знания. Закономерности изменения свойств элементов связаны с их положением в Периодической системе химических элементов Д. И. Менделеева.
Вывод: необходимо определить положение предложенных элементов в Периодической системе и описать строение их атомов.
Положение в Периодической системе и строение атомов:
- а)
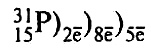 находится в третьем периоде, в главной подгруппе V группы;
находится в третьем периоде, в главной подгруппе V группы; - б)
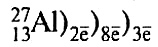 находится в третьем периоде, в главной подгруппе III группы.
находится в третьем периоде, в главной подгруппе III группы.
Проверяем справедливость сделанных утверждений.
1) Базовое знание: число электронных слоёв в атоме равно номеру периода.
Вывод: оба элемента находятся в третьем периоде, утверждение верно. Ответ 1 – правильный.
2) Базовое знание: простые вещества–неметаллы могут образовывать как двухатомные, так и многоатомные молекулы. Металлы молекул не образуют.
Вывод: алюминий – металл, утверждение неверно. Ответ 2 – неправильный.
3) Базовое знание: к металлам относятся все элементы побочных подгрупп, элементы главных подгрупп I и II групп Периодической системы (за исключением водорода и гелия) и элементы главных подгрупп, которые лежат ниже условной линии «бор – астат» (p-элементы). К неметаллам относят Н, С, N, О, F, Si, Р, S, Cl, As, Se, Br, I и инертные газы (Не, Ne, Ar, Кr, Хе, Rn).
Вывод: фосфор – неметалл (находится выше условной линии «бор – астат»), алюминий – металл. Утверждение неверно. Ответ 3 – неправильный.
4) Базовое знание: электроотрицательность элементов возрастает по периоду слева направо, то есть с увеличением номера группы. Сера находится в главной подгруппе VI группы третьего периода. Сравниваемые элементы расположены в последовательности Al → Р → S.
Вывод: электроотрицательность и фосфора, и алюминия меньше, чем серы. Утверждение верно. Ответ 4 – правильный.
Общий вывод: два правильных ответа найдены.
Ответ: 1 4
Пример 2.
Какие два утверждения верны для характеристики как азота, так и фосфора?
- 1) Во внешнем электронном слое находится пять электронов.
- 2) Соответствующее простое вещество существует в виде двухатомных молекул.
- 3) Химический элемент относится к металлам.
- 4) Значение электроотрицательности меньше, чем у сурьмы.
- 5) Химический элемент образует водородное соединение с общей формулой ЭН3.
Ответ: [ ].
Решение задания (с комментариями)
Базовые знания. Закономерности изменения свойств элементов связаны с их положением в Периодической системе химических элементов Д. И. Менделеева.
Вывод: необходимо определить положение предложенных элементов в Периодической системе и описать строение их атомов.
Положение в Периодической системе и строение атомов:
- а)
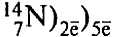 находится во втором периоде, в главной подгруппе V группы;
находится во втором периоде, в главной подгруппе V группы; - б)
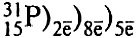 находится в третьем периоде, в главной подгруппе V группы.
находится в третьем периоде, в главной подгруппе V группы.
Проверяем справедливость сделанных утверждений.
1) Базовое знание: число электронов во внешнем слое для элементов главных подгрупп равно номеру группы.
Вывод: оба элемента находятся в главной подгруппе V группы, утверждение верно. Ответ 1 – правильный.
2) Базовое знание: азот образует простое вещество N2, для фосфора известны несколько аллотропных модификаций – белый фосфор Р4, красный фосфор, чёрный фосфор.
Вывод: утверждение неверно. Ответ 2 – неправильный.
3) Базовое знание: к металлам относятся все элементы побочных подгрупп, элементы главных подгрупп I и II групп Периодической системы (за исключением водорода и гелия) и элементы главных подгрупп, которые лежат ниже условной линии «бор – астат» (р-элементы). К неметаллам относят Н, С, N, О, F, Si, Р, S,Cl, As, Se, Вг, I.
Вывод: оба элемента в Периодической системе химических элементов Д. И. Менделеева находятся выше условной линии, «бор – астат», следовательно, азот – неметалл, фосфор – неметалл. Утверждение неправильное. Ответ 3 – неправильный.
4) Базовое знание: электроотрицательность элементов возрастает по периоду слева направо, то есть с увеличением номера группы. По группе электроотрицательность увеличивается снизу вверх.
Сурьма находится в главной подгруппе V группы пятого периода. Сравниваемые элементы расположены в последовательности N → Р → Sb.
Вывод: электроотрицательность и азота, и фосфора больше, чем сурьмы. Утверждение ошибочное. Ответ 4 – неправильный.
5) Базовое знание: элементы–неметаллы, находящиеся в одной группе, образуют летучие водородные соединения, которые имеют общую формулу.
Вывод: азот образует летучее водородное соединение NH3, фосфор – РН3, оба вещества соответствуют общей формуле ЭН3. Утверждение правильное. Ответ 5 – правильный.
Ответ: 1 5
Пример 3.
Какие два утверждения верны для ряда химических элементов Na → Mg → Al?
- 1) Уменьшаются заряды ядер атомов.
- 2) Увеличивается число электронов во внешнем электронном слое.
- 3) Уменьшается электроотрицательность.
- 4) Уменьшается радиус атомов.
- 5) Усиливаются металлические свойства.
Запишите в поле ответа номера выбранных утверждений. Ответ: [ ].
Решение задания (с комментариями)
Базовые знания. Закономерности изменения свойств элементов связаны с их положением в Периодической системе химических элементов Д. И. Менделеева.
Вывод: необходимо определить положение предложенных элементов в Периодической системе и описать строение их атомов.
Положение в Периодической системе и строение атомов:
а) ![]() , находится в третьем периоде, в главной подгруппе I группы;
, находится в третьем периоде, в главной подгруппе I группы;
б) ![]() , находится в третьем периоде, в главной подгруппе II группы;
, находится в третьем периоде, в главной подгруппе II группы;
в) ![]() , находится в третьем периоде, в главной подгруппе III группы.
, находится в третьем периоде, в главной подгруппе III группы.
Проверяем справедливость предложенных утверждений.
1) Базовое знание: заряд ядра атома равен порядковому номеру элемента.
![]()
Вывод: заряд ядра увеличивается в этом ряду, сделанное утверждение ошибочно. Ответ 1 – неправильный.
2) Базовое знание: для элементов главных подгрупп число электронов во внешнем слое равно номеру группы.
Нахождение в Периодической системе: Na (I группа) → Mg (II группа) → Al (III группа).
Число электронов во внешнем слое:
![]()
Вывод: число электронов во внешнем слое увеличивается (1ё → 2ё → 3ё), утверждение верно. Ответ 2 – правильный.
3) Базовое знание: электроотрицательность элементов возрастает по периоду слева направо, то есть с увеличением номера группы. Na (I группа) → Mg (II группа) → AI (III группа).
Вывод: электроотрицательность в этом ряду будет увеличиваться, утверждение неверно. Ответ 3 – неправильный.
4) Базовое знание: радиус атома по периоду уменьшается, то есть уменьшается с увеличением номера группы.
Na (I группа) → Mg (II группа) → Аl (III группа).
Вывод: радиус атомов в этом ряду будет уменьшаться, утверждение верно. Ответ 4 – правильный.
5) Базовые знания: металлические свойства связаны с изменением радиуса атома и электроотрицательности, по периоду металлические свойства (как и радиус атома) уменьшаются.
Вывод: металлические свойства в этом ряду будут ослабевать, утверждение ошибочно. Ответ 5 – неправильный.
Ответ: 2 4
Вы смотрели: Химия ОГЭ 2020, часть 1. Задание 6 с комментариями экспертов (разбор задания на трех примерах). Материал для подготовки к экзамену.